Aralık 2019 Bilimsel Takvimi
İmmatür trombosit oranı (IPF) cerrahiden sonra advers kardiyovasküler olaylar için nasıl bir biyobelirteç işlevi görebilir?
Periferik kanda artan trombosit tüketimi nedeniyle artan bir IPF ile normal trombosit sayımı, artan trombosit agregasyonunu ve tromboembolik komplikasyonları işaret edebilir.
Kemik iliğinde azalan trombosit üretimi nedeniyle azalan bir IPF ile trombositoz, artan trombosit agregasyonunu ve tromboembolik komplikasyonları işaret edebilir.
Periferik kanda azalan trombosit tüketimi nedeniyle azalan bir IPF ile trombositopeni, artan trombosit agregasyonunu ve tromboembolik komplikasyonları işaret edebilir.
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Bilimsel arka plan bilgisi
Koroner arter hastalıkları (CAD) en yaygın kardiyovasküler hastalıklardır. CAD, kalbe kan sağlayan arterleri etkileyen bir rahatsızlıktır. Sebebi genellikle ateroskleroz olup arterlerin daralmasına ve bunun sonucunda kan akışının yavaşlamasına neden olur.
Trombositler, aktive olmayan endotele yapışmaz. Buna karşın, ateroskleroz gibi enflamatuar olaylar trombosit tutunmasını stimüle eden endotel aktivasyonuna yol açar. Trombositler, CAD’de aterotrombozda önemli bir rol oynar: trombositler, trombus oluşumu sırasında tüketilir ve trombosit sayımı üzerindeki etki, artan yeni trombosit üretimi ile telafi edilir. Bu artan trombosit dönüşüm süreci, periferik kanda tespit edilebilen artmış immatür trombosit sayımlarıyla sonuçlanır. Dolaşımdaki immatür trombosit düzeyleri CAD hastalarında genelde yüksektir ve birkaç çalışma dolaşımdaki immatür trombositlerin oranının majör advers kardiyovasküler olaylar (MACE) ile ilişkili olduğunu göstermiştir [1-3].
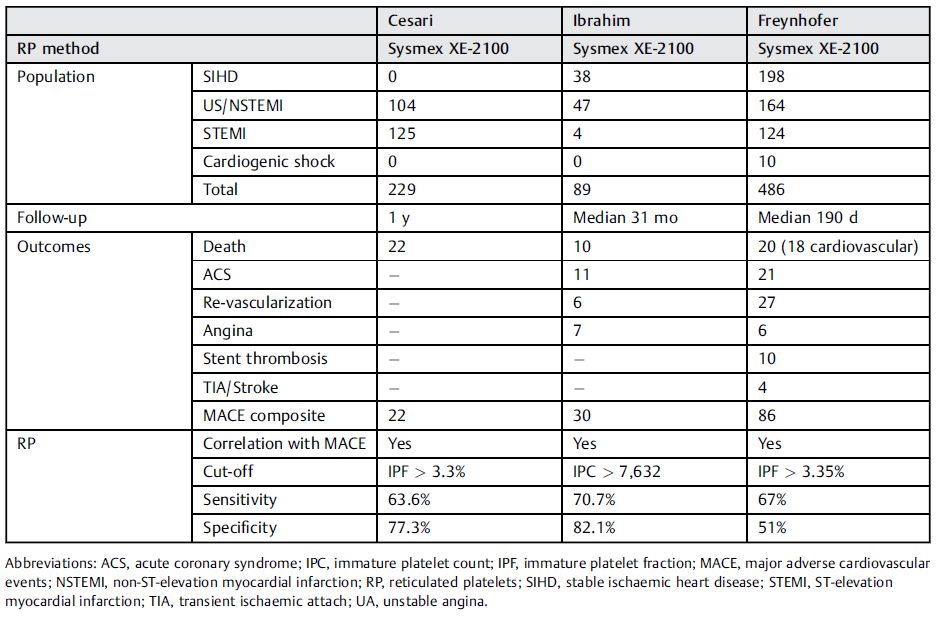
Postoperatif sonucun iyileştirilmesi için, cerrahiden sonraki komplikasyonların zamanında belirlenmesi ve sonrasında optimum şekilde yönetilmesi gerekir. MACE, yüksek mortalite oranı ile sık ve özellikle ciddi bir komplikasyon teşkil eder. Bu bağlamda, immatür trombositler MACE için potansiyel bir bağımsız prediktör olarak ilgi görmüştür [4]. İmmatür trombosit oranının (IPF) akut koroner sendromu olan hastalarda yükseldiği gösterilmiştir [5-6] ve bu hastalarda yükselen immatür trombosit sayımının cerrahiden sonra artan MACE riskiyle ilgili olduğu tespit edilmiştir [1]. Birkaç araştırmacı artan immatür trombosit oranı veya sayım değerleri ile artan ciddi kardiyovasküler olay riski arasında bir ilişki bulunduğunu bildirmiştir [1-3]. Yakın tarihli bu çalışmalardan ikisinde Sysmex IPF parametresi kullanılarak aynı eşik değeri, yani %3,3 tespit edilmiştir (Tablo 1) [7].
Yakın tarihli bir başka çalışmada, anestezi sonrası bakım ünitesinde belirlenen immatür trombosit oranının (IPF), orta ve yüksek riskli kardiyak dışı cerrahi sonrasında MACE veya diğer tromboembolik olaylar için bir prediktör olup olamayacağı değerlendirilmiştir. Kardiyak dışı cerrahi hastalarındaki bu ilk çalışmada, preoperatif dönemde, MACE olan ve olmayan hastalar arasında IPF bakımından farklılık olmadığı görülmüştür. Öte yandan, anestezi sonrası bakım ünitesinde MACE olan hastaların IPF değerleri MACE olmayan hastalara kıyasla daha yüksek bulunmuştur. IPF > %5,4 şeklindeki optimum eşik değer, eşdeğişkenlerin ayarlanmasından sonra artan bir MACE riskiyle ilişkilendirilmiştir [8]. Bu yayında ve bu ayın bilimsel takvim olgusunda gösterildiği gibi, IPF, cerrahiden sonra MACE bakımından bağımsız bir prediktördür ve kardiyak dışı cerrahi hastalarında bile risk kategorilendirmesini geliştirebilir.
İlginç bir şekilde, ışık transmisyon agregometrisi (LTA) ile ölçülen immatür trombosit reaktivitesi, MACE için prediktör görevi görmemiştir ve immatür trombositler, kısa süreli durumu yansıtması daha muhtemel olan LTA’ya göre advers olaylar açısından daha üstün kronik prediktörler olarak görünmektedir. Benzer şekilde, perkütan koroner müdahalenin ardından hastalarda immatür trombositler, vazodilatör ile stimüle edilen fosfoprotein fosforilasyonundan ya da çok plakalı elektrot agregometrisinden daha üstün MACE tahmin olanağı sağlamıştır [3].
Tablo
Referanslar
[1] Ibrahim H et al. (2014) Association of immature platelets with adverse cardiovascular outcomes. J Am Coll Cardiol. Nov 18-25; 64(20):2122–9.
[2] Cesari F et al. (2013) Reticulated platelets predict cardiovascular death in acute coronary syndrome patients. Insights from the AMI-Florence 2 Study. Thromb Haemost. May; 109(5):846–53.
[3] Freynhofer MK et al. (2017) Platelet Turnover Predicts Outcome after Coronary Intervention. Thromb Haemost. May 8; 117(5):923–33.
[4] Eikelboom JW et al. (2014) Immature platelet count: part of the cardiologist's complete blood count? J Am Coll Cardiol. Nov 18-25; 64(20):2130–2.
[5] Grove EL et al. (2009) Immature platelets in patients with acute coronary syndromes. Thromb Haemost. Jan; 101(1):151–6.
[6] Lakkis N et al. (2004) Reticulated platelets in acute coronary syndrome: a marker of platelet activity. J Am Coll Cardiol. Nov 16; 44(10):2091–3.
[7] Hannawi B et al. (2018) Reticulated Platelets: Changing Focus from Basics to Outcomes. Thromb Haemost. Sep; 118(9):1517–27.
[8] Anetsberger A et al. (2017) Immature platelets as a novel biomarker for adverse cardiovascular events in patients after non-cardiac surgery. Thromb Haemost. Oct 5; 117(10):1887–95.